美国最具声望的生物医学奖项-拉斯克奖是医学界仅次于诺贝尔奖的一项大奖,素有“美国的诺贝尔奖”、“诺贝尔奖风向标”之美誉。
1946年,由现代广告之父、美国著名广告经理人、慈善家阿尔伯特·拉斯克(Albert Lasker)及其夫人玛丽·沃德·拉斯克(Mary Woodard Lasker)共同创立,旨在表彰在医学领域作出突出贡献的科学家、医生和公共服务人员。拉斯克奖设有三个奖项:基础医学研究奖(Basic Medical Research)、临床医学研究奖(Clinical Medical Research)和公共服务奖(Public Service)。近日,拉斯克奖已揭晓2019年的获得者,下边我们就来一一欣赏这些科学桂冠上的佼佼者及其主要贡献。
2019年基础医学研究(Basic Medical Research)拉斯克奖获得者:Max D. Cooper和Jacques Miller
图片来源:http://www.laskerfoundation.orgMax D. Cooper(埃默里大学医学院)和Jacques Miller(Walter和Eliza Hall医学研究所)因其对现代免疫学的突出贡献而获得2019年基础医学研究奖。Max D. Cooper和Jacques Miller确立了两种不同类型的淋巴细胞(B细胞和T细胞)在获得性(适应性或特异性)免疫中的作用。这项开创性的工作推动了基础科学和医学科学的巨大进步,基于这一理论,单克隆抗体、抗体多样性、免疫防御、抗原加工和免疫检查点疗法得以成为现实。
大约在1960年,科学家发现了获得性免疫的一些特征,它能够保护机体免受微生物入侵,是免疫记忆的基础。在当时,已知的关键免疫活动发生在脾脏和其他淋巴组织,相比之下,尽管胸腺充满了淋巴细胞,但来自胸腺的淋巴细胞不能将免疫反应传递给其他动物,此外,从成年动物中切除胸腺也不会产生有害影响,以至于当时的人们认为胸腺是可有可无的。但Jacques Miller在攻读博士学位时发现,切除胸腺的小鼠对移植的皮肤没有排异反应,同时约三分之二的小鼠会过早死亡。Jacques Miller得出结论,胸腺是成年动物不可或缺的免疫器官。Jacques Miller还推测,胸腺可能使免疫细胞循环并使机体获得免疫能力。为了验证这一假设,他将胸腺植入胸腺切除的小鼠中,发现在受体小鼠的脾脏中,大部分分裂的淋巴细胞来自供体胸腺。正如Jacques Miller推测的那样,来自胸腺的免疫细胞可以迁移并成熟。
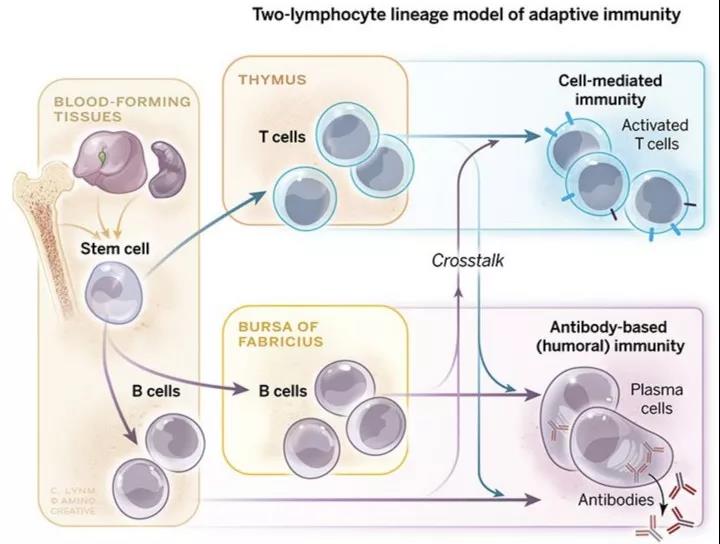
1965年和1966年,Max D. Cooper提出鸡的法氏囊是抗体生成必不可少的,而胸腺对于细胞介导的免疫反应至关重要。法氏囊和胸腺衍生的细胞最终被称为B细胞和T细胞。而B细胞和T细胞这两条路径并不是相互孤立的,事实上,每种类型细胞的信号促进了另一种类型细胞的成熟和特异化,因此形成了双通道免疫模型(Dual-armed defense system)(图1)。图1. 鸡的双通道免疫模型(Dual-armed defense system)
2019年临床医学研究(Clinical Medical Research)拉斯克奖获得者:H. Michael Shepard、Dennis J. Slamon和Axel Ullrich
图片来源:http://www.laskerfoundation.org
Michael Shepard、Dennis J. Slamon和Axel Ullrich因发明了第一种阻断致癌蛋白(HER2)的单克隆抗体Herceptin(赫赛汀),并将其发展成为乳腺癌患者的救命疗法,而获得了2019年临床医学研究奖。该疗法降低了乳腺癌复发风险、延长了转移性和早期疾病患者的生存时间。每年,美国有超过50,000名女性被诊断为HER2异常的乳腺癌,自该药问世以来,已有超过230万人接受了治疗。Michael Shepard(Genentech)和Axel Ullrich(德国Max Planck生物化学研究所)在Genentech进行了Herceptin的初步研究,Dennis J. Slamon在加利福尼亚大学洛杉矶分校(UCLA)继续深入研究。
在20世纪70年代中期,科学家发现体内基因的异常可以引发癌症。这一启示激发了这样一种观点,即扼杀这些致癌基因的活动可能会阻止它们引发的灾难。这种有针对性的治疗策略可以避免许多与化疗相关的严重副作用,同时精确杀灭肿瘤细胞。1985年,Axel Ullrich及其同事发现了一种基因,其序列类似于人类表皮生长因子受体(EGFR或HER1)。基于这种相似性,他们将其命名为HER2(人EGF受体2)。为了进一步研究HER2,Axel Ullrich和博士后研究员Robert Hudziak设计了一组实验,他们在实验室培养皿中培养小鼠结缔组织细胞,以产生额外的HER2蛋白,而这些额外的HER2蛋白使停止分裂的细胞继续分裂,表现出肿瘤状态。近乎同时,由Stuart Aaronson(美国国家癌症研究所)和Tadashi Yamamoto(东京大学)领导的另外两个小组也鉴定了HER2,并证明它在人类乳房和唾液腺的恶性肿瘤中被扩增。与此同时,加州大学洛杉矶分校的肿瘤学家Dennis J. Slamon一直在收集癌症组织,这些癌症组织由于治疗原因而被手术切除。1987年,他们报道了189个乳腺癌样本中有近30%含有一个以上的HER2基因拷贝,携带多个HER2基因拷贝的患者比只含有一个拷贝的患者复发得更快并且死亡时间更早。Michael Shepard并行地在Genentech实验室从另一个方向研究了HER2。Michael Shepard发现,HER2使小鼠细胞对肿瘤坏死因子-α(TNF-α)的毒性作用具有抗性。Michael Shepard推断,HER2不仅可以促使细胞生长,还可以增强细胞对外界因素的抵抗。
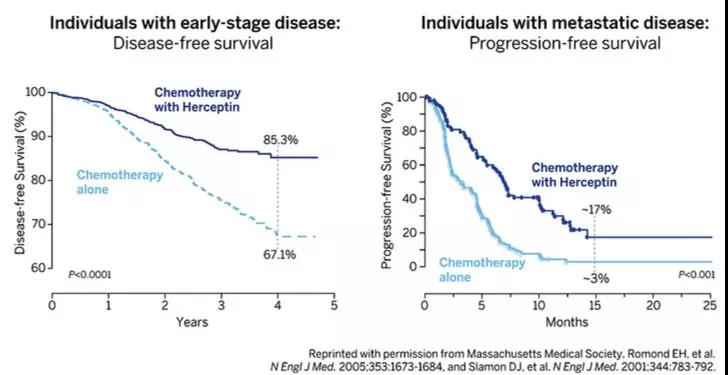
1998年,美国FDA批准了Genentech公司的人源化抗HER2单克隆抗体(曲妥珠单抗,赫赛汀)。2001年,Slamon及其同事公布了一项HER2阳性乳腺癌患者的大型临床研究,结果表明,在化疗中加入赫赛汀会使疾病进展停滞,将一年死亡率从33%降低至22%,并延长总生存期(图2)。图2. 相比于化疗,在化疗加入赫赛汀显著提高了DFS和PFS率
2019年公共服务(Public Service)拉斯克奖获得者:Gavi全球疫苗免疫联盟
图片来源:http://www.laskerfoundation.org2019年公共服务奖授予Gavi全球疫苗免疫联盟,以表彰其在全球范围内持续提供儿童疫苗,从而挽救数百万生命的贡献。Gavi全球疫苗免疫联盟确保以合理的价格提供足够的疫苗供应,加速新疫苗的开发和部署,并加强医疗保健系统。迄今为止,Gavi已帮助超过7.6亿儿童接种了疫苗,并在73个国家挽救了1300多万人的生命。比尔盖茨曾说过,“疫苗是一个奇迹”,虽然它们是科学的产物,而不是超自然的力量,但它们的影响足以触及神圣。据世界卫生组织称,免疫接种每年可防止200万至300万人死亡。
20世纪后期,世卫组织扩大免疫计划(EPI)促使疫苗接种率激增。当EPI于1974年成立时,发展中国家只有约5%的儿童接种了最基本的疫苗。到1990年,结核病、白喉、破伤风、百日咳、麻疹和脊髓灰质炎疫苗在发展中国家的接种率达到80%,但其后便停滞不前。2000年,发展中国家有近3000万儿童未完全接种疫苗,新开发的疫苗几乎没有接触到世界上最贫穷的儿童。为了解决这一问题,Gavi于2000年接受了来自比尔和梅林达盖茨基金会的7.5亿美元种子资金。其目标是通过增加低收入国家新疫苗的获取来挽救儿童生命并改善人们的健康。包括联合国儿童基金会、世界银行和世界卫生组织在内的重要机构均与Gavi进行合作,确保世界各地的儿童,无论他们住在哪里,都能从科学企业发明的强大疫苗中受益(图3)。